
Tuotteen esittely
| Pyridine Perustiedot |
| Kemiallinen rakenne Kemialliset ominaisuudet Tuotanto Käyttötarkoitukset Myrkyllisyyteen liittyvät tiedot Vaarat Viitteet |
| Tuotteen nimi: | Pyridiini |
| Synonyymit: | pyridiinikarboksyylihappo,2-(4,5-dihydro-4-metyyli-4-(1-metyylietyyli)-5-okso-1h-imidatsoli{ {9}}yyli)-5-metyyli;pyridiinikarboksyylihappo,2-(4,5-dihydro-4-metyyli-4-(1-metyylietyyli){{ 17}}okso-1h-imidatsol-2-yyli)-5-metyyli,monoammoniumsuola;Rcra-jätteen numero U196;rcrawastenumberu196;FEMA 2932;FEMA 2966;FEMA-NUMERO 2966;atsabentseeni |
| CAS: | 110-86-1 |
| MF: | C5H5N |
| MW: | 79.1 |
| EINECS: | 203-809-9 |
| Tuoteryhmät: | Meripihkanväriset lasipullot; NMR; liuotinpullot; liuotin sovelluksen mukaan; liuotin tyypin mukaan; liuotinpakkausvaihtoehdot; bioteknologian liuottimet Liuottimet; liuotinpullot; liuottimet; varma/sinetti? Pullot; Spektrofotometrinen laatu; Spektrofotometriset liuottimet; Spektroskopialiuottimet (IR; UV/Vis); Organometallit; Tributyylistanni; Kemia; PS; Alfalajittelu; Haihtuvat aineet / Puolihaihtuvat aineet; Keltaiset lasipullot; ReagentPlus(R) Liuotinlaatutuotteet; ;ACS-luokan liuottimet;CHROMASOLV PlusCHROMASOLV-liuottimet (HPLC, LC-MS);CHROMASOLV(R) Plus;LC-MS Plus ja gradientti;Aakkosellinen;P;PU - PZ;Pyridiini;Organohalogenidit;Boriesteri;Organoborons;Organosilaani;ACS GradeSemilane; -Bulkkiliuottimet;ACS-luokan liuottimet;hiiliteräspurkit, joissa on NPT-kierteet;palautettavat säiliöliuottimet;ACS- ja reagenssilaatuiset liuottimet;ReagentPlus;ReagentPlus-liuotinlaatuiset tuotteet;Biotekniset liuottimet;Sure/Seal-pullot;ACS-laatuinen reagentti;ReagenttialyyleAnalyt; ;Analyyttinen/kromatografia;Multi-Compendial;Puriss pa;Puriss pa ACS;PVC-pinnoitetut pullot;Alumiinipullot;CHROMASOLV Plus;Kromatografiareagenssit &;HPLC &;HPLC Plus Grade Liuottimet (CHROMASOLV);HPLC/UHPLCOLV-liuottimet (UCHPLCOLV); Liuottimet (CHROMASOLV);ACS-luokan liuottimet;hiiliteräspurkit NPT-kierteillä;Puolibulkkiliuottimet;halogenoidut;fluoratut;rakennuspalikat;Boorihappo;karboksi;alkoksi;Analyyttiset reagenssit yleiseen käyttöön;OP, Puriss pa;OPuris , Puriss pa ACS;Puriss pa ACS;Alumiinipullot;Aakkosellinen luettelo;Maku- ja tuoksuaineet;OP;Spektrofotometriset liuottimet;Spektrofotometriset liuottimet;PVC-pinnoitetut pullot;ReagentPlus(R)-liuotinlaatuiset tuotteet;Liuottimet };bc0001 |
| Mol-tiedosto: | 110-86-1.mol |
 |
|
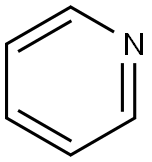
| Pyridiinin kemialliset ominaisuudet |
| Sulamispiste | -42 aste (lit.) |
| Kiehumispiste | 115 astetta (val.) |
| tiheys | 0,978 g/ml 25 asteessa (lit.) |
| höyryn tiheys | 2,72 (vs ilma) |
| Höyrynpaine | 23,8 mm Hg (25 astetta) |
| taitekerroin | n20/D 1,509 (lit.) |
| FEMA | 2966|PYRIDIINI |
| Fp | 68 astetta F |
| säilytyslämpötila | Säilytä +5 asteesta +30 asteeseen. |
| liukoisuus | H2O: mukaisesti |
| pka | 5,25 (25 asteessa) |
| muodossa | Nestemäinen |
| väri | väritön |
| Haju | Pahoinvoiva haju havaittavissa arvossa 0,23–1,9 ppm (keskiarvo=0,66 ppm) |
| Suhteellinen polariteetti | 0.302 |
| PH | 8,81 (H2O, 20 astetta) |
| räjähdysraja | 12.4% |
| Hajukynnys | 0.063 ppm |
| Hajutyyppi | hämärä |
| Vesiliukoisuus | Sekoitettava |
| Jäätymispiste | -42 astetta |
| λmax | λ: 305 nm Maksimi: 1.00 λ: 315 nm Amax: 0.15 λ: 335 nm Amax: 0.02 λ: {{0}} nm Maksimi: 0,01 |
| Merck | 14,7970 |
| BRN | 103233 |
| Henryn lain vakio | 18,4 30 asteessa (headspace-GC, Chaintreau et ai., 1995) |
| Altistumisrajat | TLV-TWA 5 ppm (-15 mg/m3) (ACGIH, MSHA ja OSHA); STEL 10 ppm (ACGIH), IDLH 3600 ppm (NIOSH). |
| Dielektrisyysvakio | 12,5 (20 astetta) |
| Vakaus: | Vakaa. Syttyvää. Yhteensopimaton vahvojen hapettimien, vahvojen happojen kanssa. |
| InChiKey | JUJWROOIHBZHMG-UHFFFAOYSA-N |
| LogP | 0.64 20 asteessa |
| CAS-tietokannan viite | 110-86-1(CAS-tietokannan viite) |
| NIST Chemistry Reference | Pyridiini (110-86-1) |
| IARC | 2B (osa 77, 119) 2019 |
| EPA-ainerekisterijärjestelmä | Pyridiini (110-86-1) |
| Turvallisuustieto |
| Vaarakoodit | T,N,F,Xn |
| Riskilausunnot | 11-20/21/22-39/23/24/25-23/24/25-52-36/38 |
| Turvallisuuslausunnot | 36/37/39-38-45-61-28A-26-28-24/25-22-36/37-16-7 |
| OEB | A |
| OEL | TWA: 5 ppm (15 mg/m3) |
| RIDADR | YK 1282 3/PG 2 |
| WGK Saksa | 2 |
| RTECS | UR8400000 |
| F | 3-10 |
| Itsesyttymislämpötila | 482 astetta |
| Vaara Huomautus | Helposti syttyvää/haitallista |
| TSCA | Joo |
| HS koodi | 2933 31 00 |
| Vaaraluokka | 3 |
| Pakkausryhmä | II |
| Vaarallisten aineiden tiedot | 110-86-1(Data vaarallisista aineista) |
| Myrkyllisyys | LD50 suun kautta rotilla: 1,58 g/kg (Smyth) |
| IDLA | 1,000 ppm |
| KTT-tiedot |
| Palveluntarjoaja | Kieli |
|---|---|
| SigmaAldrich | Englanti |
| ACROS | Englanti |
| ALFA | Englanti |
| Pyridiinin käyttö ja synteesi |
| Kemiallinen rakenne | Pyridiini on emäksinen heterosyklinen orgaaninen yhdiste, jonka kemiallinen kaava on C5H5N. Se on rakenteellisesti sukua bentseenille, ja yksi metiiniryhmä (=CH−) on korvattu typpiatomilla. Pyridiinirengas esiintyy monissa tärkeissä yhdisteissä, mukaan lukien atsiineissa ja vitamiineissa niasiini ja pyridoksiini.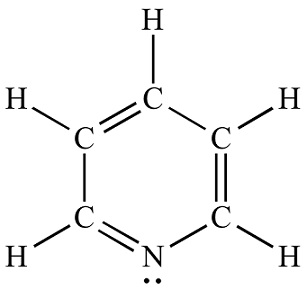 Pyridiini Lewisin rakenne |
| Kemialliset ominaisuudet | Pyridiini on väritön syttyvä neste, jolla on voimakas ja epämiellyttävä kalan haju. Pyridiini |
| Tuotokset | 2.1 Erottaminen tervasta Pyridiiniemäkset ovat tervan ainesosa. Ne eristettiin kivihiilitervasta tai kivihiilikaasusta ennen synteettisten valmistusprosessien vakiinnuttamista. Kivihiilitervan ja kivihiilikaasun sisältämät määrät ovat pieniä, ja niistä eristetyt pyridiiniemäkset ovat monien komponenttien seos. Siten, muutamaa poikkeusta lukuun ottamatta, puhtaiden pyridiiniemästen eristäminen oli kallista. Nykyään lähes kaikki pyridiiniemäkset valmistetaan synteesillä.2.2 Chichibabiinin synteesi 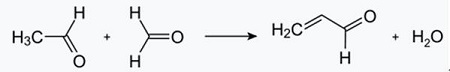 Kuva 2-1Akroleiinin muodostuminen asetaldehydistä ja formaldehydistä 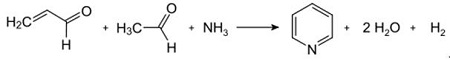 Kuva 2-2Pyridiinin kondensaatio akroleiinista ja asetaldehydistä Chichibabin pyridiinin synteesistä raportoitiin vuonna 1924, ja se on edelleen käytössä teollisuudessa. Asetaldehydi ja formaldehydi reagoivat ammoniakin kanssa muodostaen pääasiassa pyridiiniä. Ensinnäkin akroleiini muodostuu Knoevenagel-kondensaatiossa asetaldehydistä ja formaldehydistä. Sitten se kondensoidaan asetaldehydin ja ammoniakin kanssa dihydropyridiiniksi ja hapetetaan sitten kiinteän olomuodon katalyytillä pyridiiniksi. Reaktio suoritetaan yleensä lämpötilassa 350-550°C ja tilanopeudella 500-1000 h-1kiinteän happokatalyytin (esim. piidioksidi-alumiinioksidi) läsnä ollessa. Tuote koostuu pyridiinin, yksinkertaisten metyloitujen pyridiinien (pikoliini) ja lutidiinin seoksesta. Talteen otettu pyridiini erotetaan sivutuotteista monivaiheisessa prosessissa. 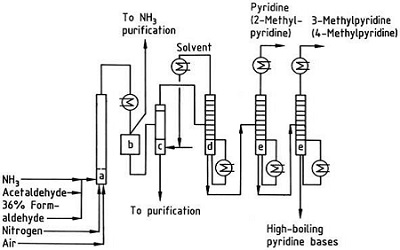 Kuva 2-3Pyridiinin ja metyylipyridiinin tuotannon virtauslevy asetaldehydistä ja formaldehydistä ammoniakilla. A) reaktori; b) Keräilijä; c) uuttaminen; d) Liuotintislaus; e) Tislaus 2.3 Alkyylipyridiinien dealkylointi Pyridiiniä voidaan valmistaa dealkyloimalla alkyloituja pyridiinejä, joita saadaan sivutuotteina muiden pyridiinien synteesissä. Oksidatiivinen dealkylointi suoritetaan joko ilmalla vanadiini(V)-oksidikatalyytin päällä, höyrydealkyloinnilla nikkelipohjaisella katalyytillä tai hydrodealkyloinnilla hopea- tai platinapohjaisella katalyytillä. Nikkelipohjaisella katalyytillä voidaan saavuttaa pyridiinin saanto jopa 93 %. 2.4 Synteesi nitriileistä ja asetyleenistä Nitriilien nestefaasireaktio asetyleenin kanssa suoritetaan lämpötilassa 120-180 ?C ja 0.8-2,5 MPa organokobolttikatalyytin läsnä ollessa ja tuottaa 2-substituoituja pyridiinejä : 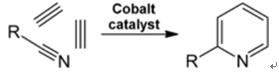 Kuva 2-42-metyylipyridiinin synteesi nitriileistä ja asetyleenistä Nitriilimolekyylin osan ja asetyleenin kahden osan trimerisaatiota pyridiiniksi kutsutaan Bönnemann-syklisaatioksi. Kun nitriilinä käytetään asetonitriiliä, saadaan 2-metyylipyridiiniä, joka voidaan dealkyloida pyridiiniksi. 2.5 Synteesi akryylinitriilistä ja ketoneista 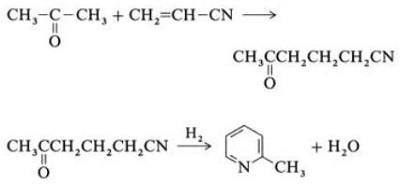 Kuva 2-52-metyylipyridiinin synteesi akryylinitriilistä ja asetonista Synteesi akryylinitriilistä ja asetonista tuottaa selektiivisesti 2-metyylipyridiiniä, joka voidaan dealkyloida pyridiiniksi. Ensinnäkin akryylinitriilin ja asetonin reaktio, jota katalysoi primaarinen alifaattinen amiini, kuten isopropyyliamiini, ja heikko happo, kuten bentsoehappo, tapahtuu nestefaasissa 180 °C:ssa ja 2,2 MPa:ssa, jolloin saadaan 5-oksoheksaaninitriiliä 91:n kanssa. % selektiivisyys. Akryylinitriilin konversio on 86%. Sitten alkutuotteen syklisointi ja dehydratointi suoritetaan kaasufaasissa vedyn läsnä ollessa palladiumia, nikkeliä tai kobolttia sisältävän katalyytin päällä 240 °C:ssa, jolloin saadaan 2-metyylipyridiiniä 84 %:n saannolla. 2.6 Synteesi dinitriileistä Höyryfaasireaktiossa nikkeliä sisältävän katalyytin päällä vedyn läsnä ollessa 2-metyyliglutaronitriili tuottaa 3-metyylipiperidiiniä, joka sitten dehydrataan palladium-alumiinioksidilla, jolloin saadaan 3-metyylipyridiiniä. Ja 3-metyylipyridiini voidaan myös dealkyloida pyridiiniksi. 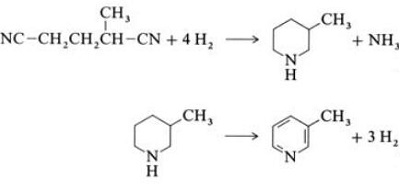 Kuva 2-62-metyylipyridiinin synteesi dinitrileistä Yksivaiheisen kaasufaasireaktion palladiumia sisältävän katalyytin päällä on raportoitu antavan 3-metyylipyridiiniä 50 %:n saannolla. 2.7 Biosynteesi Useilla pyridiinijohdannaisilla on tärkeä rooli biologisissa systeemeissä. Vaikka sen biosynteesiä ei täysin ymmärretä, nikotiinihappoa (B3-vitamiinia) esiintyy joissakin bakteereissa, sienissä ja nisäkkäissä. Nisäkkäät syntetisoivat nikotiinihappoa hapettamalla aminohappo tryptofaani, jolloin välituote, aniliini, muodostaa pyridiinijohdannaisen, kinureniinin. Päinvastoin, Mycobacterium tuberculosis- ja Escherichia coli -bakteerit tuottavat nikotiinihappoa glyseraldehydi-3-fosfaatin ja asparagiinihapon kondensoimalla. 2.8 Muut menetelmät Eteeni ja ammoniakki reagoivat palladiumkompleksikatalyytin läsnä ollessa, jolloin saadaan 2-metyylipyridiiniä ja MEP:tä. Pyridiini voidaan valmistaa syklopentadieenista ammoksidoimalla tai 2-penteenenitriilistä syklisoimalla ja dehydraamalla. Furfuryylialkoholi tai furfuraali reagoi kaasufaasissa olevan ammoniakin kanssa muodostaen pyridiiniä. 2-Metyylipyridiiniä valmistetaan myös aniliinista. |
| Käyttää | 3.1 Liuotin Pyridiini (110-86-1) on polaarinen, emäksinen, vähän reaktiivinen liuotin, erityisesti dehydrokloorausreaktioihin ja antibioottien uuttamiseen. Eliminaatioreaktiossa pyridiini toimii eliminaatioreaktion emäksenä ja sitoo tuloksena olevan halogenidin muodostaen pyridiniumsuolan. Esteröinnissä ja asyloinnissa pyridiini aktivoi karboksyylihappohalogenideja tai -anhydridejä. 3.2 Lääkkeet Pyridiinin kemiallinen rakenne löytyy erilaisista lääkkeistä, jotka syntetisoidaan osittain pyridiinin ansiosta. Yksi esimerkki on esomepratsoli-niminen lääke, joka on Nexiumin yleisnimi. Tämä on lääke, jota käytetään GERD:n tai gastroesofageaalisen refluksitaudin hoitoon. Toinen esimerkki pyridiiniä sisältävästä lääkkeestä on loratadiini, joka tunnetaan yleisemmin tuotenimellään Claritin. Loratadiini auttaa allergioiden hoidossa. 3.3 Torjunta-aineet Pyridiinin pääasiallinen käyttö on parakvatin ja dikvatin rikkakasvien torjunta-aineiden esiaste. Klooripyrifossin hyönteismyrkkyjen ensimmäinen synteesivaihe koostuu pyridiinin kloorauksesta. Pyridiini on myös lähtöaine pyritionipohjaisten fungisidien valmistuksessa. Setyylipyridiniumia ja lauryylipyridiniumia, joita voidaan valmistaa pyridiinistä Zincke-reaktiolla, käytetään antiseptisenä aineena suun ja hampaiden hoitotuotteissa. Alkyloivat aineet hyökkäävät helposti pyridiiniin, jolloin muodostuu N-alkyylipyridiniumsuoloja. Yksi esimerkki on setyylipyridiniumkloridi.  Kuva 3-1 Paraquatin synteesi 3.4 Piperidiinin synteesi Piperidiini, perustavanlaatuinen typen heterosykli, on tärkeä synteettinen rakennusaine. Piperidiinejä valmistetaan hydraamalla pyridiiniä nikkeli-, koboltti- tai ruteenipohjaisella katalyytillä korotetuissa lämpötiloissa. C5H5N + 3 H2 → C5H10NH3.5 Ligandin ja Lewisin tukikohta Pyridiiniä käytetään laajalti ligandina koordinaatiokemiassa. Metallikompleksin ligandina se voidaan helposti korvata vahvemmalla Lewis-emäksellä, jota voidaan käyttää polymerointi- ja hydrausreaktioiden katalyysissä. Reaktion päätyttyä reaktion aikana korvattu pyridiiniligandi voidaan palauttaa uudelleen. Pyridiiniä käytetään myös emäksenä kondensaatioreaktioissa. Emäksenä pyridiiniä voidaan käyttää Karl Fischer -reagenssina, mutta se korvataan yleensä mieluisamman tuoksuisilla vaihtoehdoilla, kuten imidatsolilla. 3.6 Muut Edellä mainittuja käyttötarkoituksia lukuun ottamatta pyridiiniä käytetään myös polykarbonaattihartsien, vitamiinien, elintarvikearomien, maalien, väriaineiden, kumituotteiden, liimojen ja kankaiden vedeneristysaineiden valmistukseen. Pyridiiniä lisätään etanoliin, jotta se ei sovellu juotavaksi. Sitä käytetään myös DNA:n in vitro -synteesissä. |
| Myrkyllisyystiedot | 4.1 Myrkyllisyystaso Matala toksisuus 4.2 Välitön myrkyllisyys LD501580mg/kg (suuret hiiret, suun kautta); 1121 mg/kg (kani, ihon läpi); ihmisen hengitettynä 25mg/m3×20 min, sidekalvon ja ylempien hengitysteiden limakalvojen ärsytys. Subakuutti ja krooninen toksisuus: suuret hiiret hengittävät 32,3 mg/m3 × 7 tuntia/päivä x 5 päivää/viikko x 6 kuukautta, maksan painon nousu; ihmisten hengittämä 20-40mg/m3 (pitkäaikainen), hermovaurio, epävakaa kävely, digitaalinen vapina, alhainen verenpaine, liiallinen hikoilu, satunnainen maksa- ja munuaisvaurio. |
| Vaarat | 5.1 Terveysvaarat Pyridiini on erittäin myrkyllistä nieltynä ja hengitettynä. Höyryt ovat ilmaa raskaampia. sen palaessa muodostuu myrkyllisiä typen oksideja. Pyridiini on erittäin syttyvää (sen leimahduspiste on vain 17 ºC). Pyridiinillä voi myös olla neurotoksisia ja genotoksisia vaikutuksia. 5.2 Palovaarat Käyttäytyminen tulessa: Höyry on ilmaa raskaampaa ja voi kulkea huomattavan matkan sytytyslähteeseen ja leimahtaa takaisin. |
| Viitteet |
https://en.wikipedia.org/wiki/Pyridine#Occurrence http://www.zwbk.org/MyLemmaShow.aspx?zh=zh-tw&lid=169038 http://www.softschools.com/formulas/chemistry/pyridine{0}}formula/378/ http://www.hmdb.ca/metabolites/HMDB0000926 https://study.com/academy/lesson/pyridine-in-medicine-uses-synthesis.html#partialRegFormModal http://www.toxipedia.org/display/toxipedia/Pyridine https://www.chemicalbook.com/ProductChemicalPropertiesCB8852825_EN.htm https://pubchem.ncbi.nlm.nih.gov/compound/pyridine#section=Alkuun http://www.ebi.ac.uk/chebi/searchId.do;jsessionid=E7088896622D62FC650863C2AD197CAA?chebiId=CHEBI:16227 https://www.britannica.com/science/pyridine Shimizu, S.; Watanabe, N.; Kataoka, T.; Shoji, T.; Abe, N.; Morishita, S.; Ichimura, H. (2005), "Pyridine and Pyridine Derivatives", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi: 10.1002/14356007.a22_399 |
| Kemialliset ominaisuudet | Pyridiini on hieman keltainen tai väritön neste; hygroskooppinen; epämiellyttävä haju; polttava maku; reaktiossa lievästi emäksinen; liukenee veteen, alkoholiin, eetteriin, bentseeniin ja rasvaöljyihin; ominaispaino, 0,978; itsesyttymislämpötila, 482 astetta. Pyridiini, tertiäärinen amiini, on jonkin verran vahvempi emäs kuin aniliini ja muodostaa helposti kvaternaarisia ammoniumsuoloja. |
| Kemialliset ominaisuudet | Pyridiini on heikko emäs (pKa{{0}}.25); 0,2 M liuoksen pH on 8,5 (HSDB 1988). Sen hiiliatomit deaktivoituvat kohti elektrofiilistä substituutiota. Tämä pätee erityisesti happamissa väliaineissa, joissa typessä muodostuu suoloja. Se käy kuitenkin helposti läpi nukleofiilisen substituution, ensisijaisesti C-2- ja myös C-4-asemassa (Jori et al 1983). Tertiäärisenä amiinina pyridiini reagoi alkyloivien aineiden kanssa muodostaen kvaternäärisiä suoloja (Santodonato et al 1985). Koska sen kyky luovuttaa elektroneja on pienempi, se kestää paremmin hapettumista kuin bentseeni. Hapetus peroksihapoilla muodostaa pyridiini-N-oksidia, joka pystyy sitten käymään läpi elektrofiilisen substituution (Jori et al 1983). Pyridiini reagoi kiivaasti useiden yhdisteiden kanssa, mukaan lukien typpihappo, rikkihappo, maleiinihappoanhydridi, perkromaatti, beeta-propiolaktoni ja kloorisulfonihappo. Terminen hajoaminen voi vapauttaa syanideja (Gehring 1983). Sekä pyridinium-ioni että itse pyridiini pelkistyvät helposti kaupallisesti tärkeäksi yhdisteeksi, piperidiiniksi (Jori et ai. 1983). |
| Fyysiset ominaisuudet | Kirkas, väritön tai vaaleankeltainen, syttyvä neste, jolla on terävä, läpäisevä, pahoinvoiva kalan haju. Hajukynnyspitoisuudet vedessä ja ilmassa olivat 2 ppm (Buttery et al., 1988) ja 21 ppbv(Leonardos et ai., 1969), vastaavasti. Havaitsemishajukynnyspitoisuudet 0,74 mg/m3(2,3 ppmv) ja 6 mg/m3(1,9 ppmv) määrittivät kokeellisesti Katz ja Talbert (1930) ja Dravnieks (1974). Cometto-Mu?iz ja Cain (1990) raportoivat, että nenän keskimääräinen pistävä kynnyspitoisuus oli 1 275 ppmv. |
| Esiintyminen | Anderson löysi pyridiinin kivihiilitervasta vuonna 1846 (Windholz et al 1983). Sitä löytyy tupakansavusta (Vohl ja Eulenberg 1871; Lehmann 1909) ja paahdetusta kahvista (Bertrand ja Weisweiller 1913). Pyridiiniä löytyy puuöljystä ja Atropa belladonnan lehdistä ja juurista (HSDB 1988), ja se on myös kreosoottiöljyn komponentti (Krone et al 1986). Luonnossa pyridiiniä ja sen johdannaisia esiintyy yleisesti alkaloidien, vitamiinien ja koentsyymien komponentteina. |
| Käyttää | Pyridiiniä käytetään liuottimena maali- ja kumiteollisuudessa; välituotteena väriaineissa ja lääkkeissä; alkoholin denaturointiin ja reagenssina syanidianalyysiin. Sitä esiintyy kivihiilitervassa. |
| Käyttää | Pyridiiniä käytetään suoraan alkoholin denaturoinnissa (ACGIH 1986; HSDB 1989; NSC 1978) ja liuottimena maalin- ja kumin valmistuksessa (ACGIH 1986; HSDB 1989; NSC 1978) sekä tutkimuslaboratorioissa toimintoihin, kuten kasvihormonien erottamiseen ( Santodonato et ai. 1985). Puolet nykyään tuotetusta pyridiinistä käytetään välituotteena erilaisten hyönteismyrkkyjen ja rikkakasvien torjunta-aineiden valmistuksessa maataloussovelluksiin (ACGIH 1986; Harper et al. 1985; Santodonato et al. 1985). Noin 20 % menee piperidiinin tuotantoon (Harper et al. 1985; Santodonato et al. 1985), joka on kaupallisesti merkittävä kumin vulkanoinnissa ja maataloudessa käytettävien kemikaalien valmistuksessa (NSC 1978). Pyridiiniä käytetään myös välituotteena lääkkeiden (antihistamiinit, steroidit, sulfa-tyyppiset ja muut antibakteeriset aineet) väriaineiden, vettä hylkivien aineiden ja polykarbonaattihartsien valmistuksessa (ACGIH 1986; Harper et al. 1985; NSC 1978; Santodonato et al. 1985). Food and Drug Administration (FDA) on myös hyväksynyt pyridiinin käytettäväksi aromiaineena elintarvikkeiden valmistuksessa (Harper et ai. 1985; HSDB 1989). |
| Määritelmä | ChEBI: Pyridiini on atsaareeni, joka sisältää bentseeniytimen, jossa yksi -CH-ryhmä on korvattu typpiatomilla. Se on pyridiinien luokan emoyhdiste. Molekyyleillä on kuusikulmainen tasorengas ja ne ovat isoelektronisia bentseenin kanssa. Pyridiini on esimerkki aromaattisesta heterosyklisestä yhdisteestä, jossa elektronit hiili-hiili pi-sidoksissa ja typen yksinäinen pari on siirretty atomirenkaan yli. Yhdiste uutetaan kivihiilitervasta ja sitä käytetään liuottimena ja orgaanisen synteesin raaka-aineena. |
| Tuotantomenetelmät | Pyridiiniä valmistetaan kaasuista, joita saadaan kivihiilen koksaamisesta ja suorasta synteesistä. Kivihiilitervan kevytöljyfraktiota käsitellään rikkihapolla vesiliukoisten pyridiinisuolojen tuottamiseksi ja sitten pyridiiniemäkset otetaan talteen vesifaasista natriumhydroksidilla tai ammoniakilla (Jori et al 1983). Suurin osa Yhdysvaltojen tuotannosta tapahtuu synteettisin keinoin. Tässä prosessissa käytetään asetaldehydin, formaldehydin ja ammoniakin höyryfaasireaktiota, joka tuottaa pyridiinin ja 3-metyylipyridiinin seoksen (Santodonato et al 1985). Tuotesuhde riippuu asetaldehydin ja formaldehydin suhteellisista määristä. Lisätty metanoli lisää saantoa. Pyridiinin USA:n tuotannon arvioitiin olevan 32-47 miljoonaa puntaa vuonna 1975 (Reinhardt ja Brittelli 1981). Pyridiiniä on kaupallisesti saatavilla teknisinä, 2 asteen ja 1 asteen laatuina, joista kaksi jälkimmäistä viittaavat niiden kiehumisalueisiin. Tärkeimmät epäpuhtaudet ovat korkeammalla kiehuvat homologit, kuten pikoliinit, lutidiinit ja kollidiinit, jotka ovat mono-, di- ja trimetyylipyridiinejä (Santodonato et al 1985; Jori et al 1983). |
| Valmistautuminen | Pyridiiniä tuotetaan joko eristämällä luonnollisista lähteistä, kuten kivihiilestä, tai kemiallisella synteesillä (HSDB 1989). Pyridiiniä tuotetaan jakotislaamalla kivihiilitervajäännöksiä (HSDB 1989; NSC 1978; Santodonato et al. 1985), jossa 1 tonni kivihiiltä tuottaa 0.07-0.21 paunaa pyridiiniemäksiä josta 57 % on pyridiiniä (Santodonato et ai, 1985). Synteettisesti valmistettu pyridiini on tällä hetkellä tärkeämpi pyridiinin lähde kaupallisiin käyttötarkoituksiin (Santodonato et ai. 1985). Pieniä määriä pyridiiniä syntetisoidaan asetaldehydistä, formaldehydistä ja ammoniakista leijutetulla piidioksidi-alumiinioksidikatalyytillä, mitä seuraa fraktiointi pyridiinin eristämiseksi (Harper et ai. 1985; HSDB 1989; NSC 1978). Pyridiiniä tuottaa luonnollisista lähteistä Crowley Tar Products, Stow, Ohio, ja Oklahoma City, Oklahoma (Harper et ai. 1985; HSDB 1989; SRI 1986, 1987, 1988). Pyridiiniä tuottaa synteettisesti kaksi yritystä, Nepera Chemical Co. of Harriman, New York ja Reilly Tar ja Chemical Corporation of Indianapolis, Indiana (Harper et ai. 1985; SRI 1986, 1987, 1988). |
| Aromikynnysarvot | Tunnistus: 0.079 - 790 ppb; tunnistus: 7,9 - 40 ppm |
| Yleinen kuvaus | Kirkas väritön tai vaaleankeltainen neste, jolla on tunkeutuva, pahoinvoiva haju. Tiheys 0,978 g / cm3. Leimahduspiste 68° F. Höyryt ovat ilmaa raskaampia. Myrkyllistä nieltynä ja hengitettynä. Palaminen tuottaa myrkyllisiä typen oksideja. |
| Ilman ja veden reaktiot | Helposti syttyvää. Liukenee veteen. |
| Reaktiivisuusprofiili | Atsabentseeni on emäs. Reagoi eksotermisesti happojen kanssa. Valmistettaessa kompleksia atsabentseeni kromitrioksidin, hapon kanssa, kromitrioksidin osuutta lisättiin. Tämän happo-emäsreaktion aiheuttama kuumeneminen johti räjähdykseen ja tulipaloon [MCA-tapaushistoria 1284 1967]. 0,1-prosenttinen atsabentseenin (tai muun tertiäärisen amiinin) liuos maleiinihappoanhydridissä 185 asteessa antaa eksotermisen hajoamisen ja kaasun nopean kehittymisen [Chem Eng. Uutiset 42(8); 41 1964]. Atsabentseenin sekoittaminen yhtä suurissa molaarisissa annoksissa minkä tahansa seuraavista aineista suljetussa astiassa aiheutti lämpötilan ja paineen nousun: kloorisulfonihappo, typpihappo (70 %), oleum, rikkihappo (96 %) tai propiolaktoni [NFPA 1991]. Jodin, atsabentseenin, rikkitrioksidin ja formamidin yhdistelmä kehitti ylipaineisen kaasun useiden kuukausien jälkeen. Tämä johtui rikkihapon hitaasta muodostumisesta ulkoisesta vedestä tai formamidin dehydraatiosta vetysyanidiksi. Etyleenioksidi ja SO2 voivat reagoida kiivaasti atsabentseeniliuoksessa paineistuksen kanssa, jos etyleenioksidia on ylimäärä (Nolan, 1983, Case History 51). |
| Vaara | Syttyvä, vaarallinen palovaara, räjähdysrajat ilmassa 1,8–12,4 %. Myrkyllistä nieltynä ja hengitettynä. Ihoa ärsyttävä, maksa- ja munuaisvaurioita aiheuttava aine. Kyseenalainen syöpää aiheuttava aine. |
| Terveysvaara | Pyridiinin akuutti toksisuus on alhainen. Hengitys ärsyttää hengityselimiä ja voi vaikuttaa keskushermostoon aiheuttaen päänsärkyä, pahoinvointia, oksentelua, huimausta ja hermostuneisuutta. Pyridiini ärsyttää silmiä ja ihoa ja imeytyy helposti, mikä johtaa systeemisiin vaikutuksiin. Pyridiinin nieleminen voi aiheuttaa maksa- ja munuaisvaurioita. Pyridiini aiheuttaa hajuväsymystä, eikä sen haju anna riittävää varoitusta haitallisista pitoisuuksista. Pyridiinin ei ole todettu olevan syöpää aiheuttava eikä sillä ole lisääntymis- tai kehitystoksisuutta ihmisillä. Pitkäaikainen altistuminen pyridiinille voi johtaa maksan, munuaisten ja keskushermoston vaurioitumiseen. |
| Terveysvaara | Pyridiinin myrkyllisiä vaikutuksia ovat päänsärky, huimaus, hermostuneisuus, pahoinvointi, unettomuus, tiheä virtsaaminen ja vatsakipu. Oireet olivat ohimeneviä, esiintyivät ihmisillä subakuutista altistumisesta pyridiinihöyryille noin 125 ppm 4 tuntia päivässä 1–2 viikon ajan (Reinhardt). ja Brittelli 1981). Pyridiinimyrkyllisyyden kohde-elimet ovat keskushermosto, maksa, munuaiset, maha-suolikanava ja iho. Altistumisreitit ovat höyryjen hengittäminen ja nesteen nieleminen ja imeytyminen ihon läpi. Krooninen hengittäminen voi aiheuttaa vakavia terveysriskejä, jotka voivat aiheuttaa munuais- ja maksavaurioita, ja luuytimen stimulaatio lisäämään verihiutaleiden tuotantoa. Pieni, 10 ppm:n altistuminen voi aiheuttaa kroonisia myrkytysvaikutuksia keskushermostoon. Nesteen nieleminen voi aiheuttaa samoja oireita kuin yllä mainitut. Ihokosketus voi aiheuttaa ihotulehduksen. Höyry ärsyttää silmiä, nenää ja keuhkoja. Voimakkaan epämiellyttävän hajun vuoksi on aina riittävä varoitus ylialtistumisesta. 10 ppm:n pitoisuus on ihmiselle vastenmielinen. LCLO-arvo, sisäänhengitys (rotat): 4000 ppm/4 h LD50-arvo, suun kautta (hiiret): 1500 mg/kg. Huh ja työtoverit (1986) ovat tutkineet glykyrretiinihapon vaikutusta pyridiinitoksisuuteen hiirillä. Esikäsittely glykyrretiinihapolla vähensi keskushermoston lamaa ja pyridiinin aiheuttamaa kuolleisuutta eläimillä. Tällainen esikäsittely vähensi merkittävästi seerumin transaminaasientsyymin aktiivisuutta ja lisäsi maksan mikrosomaalisen aniliinihydroksylaasin [9012-90-0], pyridiiniä metaboloivan entsyymin, aktiivisuutta. |
| Syttyvyys ja räjähtävyys | Pyridiini on helposti syttyvä neste (NFPA-luokitus=3), ja sen höyryt voivat kulkea huomattavan matkan ja "palaa takaisin". Pyridiinihöyry muodostaa räjähtäviä seoksia ilman kanssa pitoisuuksina 1,8 - 12,4 % (tilavuus). Pyridiinipaloissa tulee käyttää hiilidioksidi- tai kuivasammuttimia. |
| Teolliset käyttötarkoitukset | Pyridiini on hyvä liuotin useille yhdisteille, sekä orgaanisille että epäorgaanisille (Windholz et al 1983). Noin 50 % Yhdysvalloissa käytetystä pyridiinistä on tarkoitettu maatalouskemikaalien, kuten rikkakasvien torjunta-aineiden parakvatin, dikvatin ja triklopyyrin sekä hyönteismyrkkyjen klooripyrifossin, tuotantoon. Muita käyttötarkoituksia ovat piperidiinin tuotanto; lääkkeiden, kuten steroidien, vitamiinien ja antihistamiinien, valmistus; ja liuottimena. Liuottimia käytetään sekä lääke- että polykarbonaattihartsiteollisuudessa. Se on erityisen käyttökelpoinen liuottimena prosesseissa, joissa HCl:tä kehittyy (Santodonato et al 1985). Pyridiiniä käytetään vähäisemmässä määrin alkoholin ja pakkasnesteen seosten denaturointiin, tekstiilien värjäysapuaineena ja aromiaineena (Jori et al 1983; Furia 1968; HSDB 1988). |
| Ota yhteyttä allergeeneihin | Pyridiiniä (substituoimaton pyridiini) ja sen johdannaisia (substituoidut pyridiinit) käytetään laajalti kemiassa. Pyridiini on liuotin, jota käytetään monille orgaanisille yhdisteille ja vedettömille metallisuolakemikaaleille. Karl Fischer -reagenssissa se aiheutti kosketusihottuman laboratorioteknikolle. Ristiherkkyyttä näiden eri aineiden välillä ei havaita. |
| Turvallisuusprofiili | Myrkytys intraperitoneaalisesti. Kohtalaisen myrkyllistä nieltynä, ihokosketuksessa, laskimoon ja ihon alle. Lievästi myrkyllistä hengitettynä. Ärsyttää voimakkaasti ihoa ja silmiä. Mutaatiotiedot raportoitu. Voi aiheuttaa keskushermoston lamaa, maha-suolikanavan häiriöitä sekä maksa- ja munuaisvaurioita. Syttyvä neste ja vaarallinen tulipalon vaara altistuessaan kuumuudelle, liekille tai hapettimille. Vakava räjähdysvaara höyryn muodossa, kun se altistuu liekille tai kipinöille. Reagoi kiivaasti kloorisulfonihapon, kromitrioksidin, typpitetraoksidin, HNO3:n, oleumin, perkromaattien, ppropiolaktonin, AgClO4:n, H2SO4:n kanssa. Hehkulamppureaktio fluorin kanssa. Reagoi muodostaen pyroforisia tai räjähtäviä tuotteita bromitrifluoridin, trifluorimetyylihypofluoriitin kanssa. Formamidin + jodin + rikkitrioksidin seokset ovat varastointivaarallisia ja vapauttavat hiilidioksidia ja rikkihappoa. Yhteensopimaton hapettavien materiaalien kanssa. Reagoi maleiinihappoanhydridin kanssa (yli 150 astetta) kehittäen hiilidioksidia. Käytä palon sammuttamiseen alkoholivaahtoa. Kuumennettaessa hajoamiseen se vapauttaa erittäin myrkyllisiä NOx-höyryjä. |
| Mahdollinen altistuminen | Pyridiiniä käytetään liuottimena kemianteollisuudessa ja etyylialkoholin denaturointiaineena; välituotteena torjunta-aineiden tuotannossa; lääkkeissä; maalien, räjähteiden, väriaineiden, kumin, vitamiinien, sulfalääkkeiden valmistuksessa; ja desinfiointiaineet. |
| Karsinogeenisuus | Pyridiini ei ollut karsinogeeninen useissa kroonisissa ihonalaisissa tutkimuksissa. F344-rotille annettiin pyridiiniä suun kautta juomavedessä annoksina 0, 7, 14 tai 33 mg/kg 2 vuoden ajan. Huippuannos sai aikaan painon ja vedenkulutuksen laskun. Miehillä havaittiin lisääntynyttä munuaisten tubulusadenomaa tai karsinoomaa ja tubulushyperplasiaa annoksella 33 mg/kg. Lisääntynyt mononukleaarinen soluleukemia havaittiin naarailla annoksilla 14 ja 33 mg/kg, mitä pidettiin epäselvänä pyridiinialtistuksen suhteen, koska tämä on yleinen löydös tässä rottakannassa. Pitoisuuteen liittyvä ei-neoplastinen muutos maksassa havaittiin annoksella 33 mg/kg. Urospuolisia Wistar-rottia hoidettiin samalla tavalla annoksilla 0, 8, 17 tai 36 mg/kg 2 vuoden ajan. Eloonjäämisen ja painon vähenemistä havaittiin annoksilla 17 ja 36 mg/kg. Lisääntynyttä kivessoluadenoomia havaittiin annoksella 36 mg/kg. Muissa kudoksissa, mukaan lukien munuaiset, ei raportoitu muutoksia eloonjäämismäärissä tai kasvainten määrässä, vaikka joillakin pyridiinillä hoidetuilla rotilla havaittiin lisääntynyttä nefropatiaa ja maksan sentrilobulaarista rappeutumista/nekroosia. |
| Lähde | Pyridiiniä esiintyy luonnostaan perunoissa, anabisissa, kananlehdissä, piparminttuissa (0 - 1 ppb), teelehdissä ja tupakanlehdissä (Duke, 1992). Tunnistettu yhdeksi käytettyjen soijaöljyjen 140 haihtuvasta ainesosasta, jotka on kerätty käsittelylaitoksesta, joka paistoi erilaisia naudan-, kana- ja vasikanlihatuotteita (Takeoka et al., 1996). |
| Ympäristön kohtalo | Biologinen.Heukelekian ja Rand (1955) raportoivat 5-d BOD-arvon 1,31 g/g, mikä on 58,7 % ThOD-arvosta 2,23 g/g. Nocardia sp. maaperästä eristetty kykeni muuttamaan pyridiinin semikarbatsidin läsnä ollessa välituotteeksi, joka tunnistettiin meripihkahapon semialdehydiksi (Shukla ja Kaul, 1986). 1,4-Dihydropyridiini, glutaaridialdehydi, glutaarihapon semialdehydi ja glutaarihappo tunnistettiin välituotteina, kun Nocardia-kanta Z1 hajotti pyridiinin (Watson ja Cain, 1975). Fotolyyttinen.Vesiliuoksen säteilytys 50 asteessa 24 tunnin ajan johti 23,06 %:n hiilidioksidisaantoon (Knoevenagel ja Himmelreich, 1976). Kemiallinen/Fysikaalinen.Otsonin kaasufaasireaktio pyridiinin kanssa synteettisessä ilmassa 23 asteessa tuotti nitrattua suolaa, jonka kaava on: [C6H5NH]+NO3 - (Atkinson et ai., 1987). Pyridiinin otsonointia vesiliuoksissa 25 asteessa tutkittiin tert-butyylialkoholin (20 mM) lisäyksen kanssa radikaalin sieppaajana ja ilman sitä. Tert-butyylialkoholilla pyridiinin otsonointi tuotti pääosin pyridiini-N-oksidia (saanto 80 %), joka oli erittäin stabiili otsonin suhteen. Ilman tert-butyylialkoholia heterosyklinen rengas lohkeaa nopeasti muodostaen ammoniakkia, nitraattia ja amidiyhdistettä N-formyylioksaamihappoa (Andreozzi et ai., 1991). |
| Aineenvaihdunta | Pyridiini imeytyy maha-suolikanavan, ihon ja keuhkojen kautta ja eliminoituu virtsan, ulosteiden, ihon ja keuhkojen kautta sekä metaboliitteina että lähtöaineena (Jori et al 1983). Kudosten sisäänotto lisääntyy annoksen myötä ja eliminaatio on luonteeltaan kaksivaiheista (Zharikov ja Titov 1982; HSDB 1988). Eliminaatio on nopeaa, eikä kudosten kertymistä näytä tapahtuvan (Jori et al 1983). Hisin (1887) havainto Af-metyylipyridiinin virtsaan erittymisestä pyridiinia saaneista eläimistä oli ensimmäinen esimerkki Af-metylaatiosta. Tunnettuja pyridiinin virtsan metaboliitteja nisäkkäillä ovat nykyään pyridiini-N-oksidi, N-metyylipyridiini, 4-pyridoni, 2-pyridoni ja 3-hydroksipyridiini. Jotkut metaboliitit ovat vielä tunnistamatta (Damani et al 1982). Metaboliittien suhteellinen määrä riippuu suuresti lajista ja annoksesta (Gorrod ja Damani 1980). Esimerkiksi rotan on osoitettu erittävän 70 % annoksesta 1 mg/kg virtsaan ensimmäisten 24 tunnin aikana annostelun jälkeen, mutta tämä luku putoaa vain 5,8 %:iin 500 mg/kg annoksella (D'Souza et). al 1980). Vaikka pyridiinin ja sen metaboliittien erittyminen virtsaan näyttää olevan tärkein eliminaatioreitti, ei-virtsaa erittymistä ei ole tutkittu laajasti (Santodonato et al 1985). Kaneissa pyridiini-N-metyylitransferaasiaktiivisuuden on osoitettu olevan suurin keuhkojen sytosolissa, ja sen on havaittu hyödyntävän 5-adenosyylimetioniinia metyyliluovuttajana (Damani et al 1986). Tämä reitti on kyllästyvä sekä rotalla että marsulla (D'Souza et al 1980). Tämän reaktion tuote, N-metyylipyridiini, on vähemmän kroonisesti toksinen, mutta akuutimmin myrkyllinen kuin pyridiini (Williams 1959). Pyridiini-N-oksidia tuottaa sytokromi P-450-järjestelmä ja aktiivisuus indusoituu fenobarbitaali- tai pyridiiniesikäsittelyllä, mutta ei 3-metyylikolantreenilla (Gorrod ja Damani 1979; Kaul ja Novak 1987). Kanilla alkoholilla indusoituva (ja pyridiinin indusoituva) P-450 LM3Anäyttää olevan alhainen Kmisotsyymi, joka katalysoi pyridiini-Af-oksidin tuotantoa (Kim ja Novak 1989). Pyridiinin N-hapetus voi edustaa polkua bioaktivaatioon (Santodonato et al 1985), ja tästä reitistä tulee tärkeämpi pyridiiniannosta kasvatettaessa (Damani et al 1982). |
| varastointi | Pyridiiniä tulee käyttää vain alueilla, joissa ei ole sytytyslähteitä, ja yli 1 litran määrät tulee säilyttää tiiviisti suljetuissa metallisäiliöissä erillään hapettimista. |
| laivaus | UN1992 Syttyvät nesteet, myrkylliset, nos, Vaaraluokka: 3; Tarrat: 3-Syttyvä neste, 6.1-Myrkylliset materiaalit, tekninen nimi vaaditaan. |
| Puhdistusmenetelmät | Todennäköisiä epäpuhtauksia ovat H2O ja amiinit, kuten pikoliinit ja lutidiinit. Pyridiini on hygroskooppinen ja sekoittuu H2O:n ja orgaanisten liuottimien kanssa. Se voidaan kuivata kiinteällä KOH:lla, NaOH:lla, CaO:lla, BaO:lla tai natriumilla, mitä seuraa jakotislaus. Muita kuivausmenetelmiä ovat seisominen Linden tyypin 4A molekyyliseuloilla, CaH2:lla tai LiAlH4:llä, H2O:n atseotrooppinen tislaus tolueenilla tai *bentseenillä tai käsittely fenyylimagnesiumbromidilla eetterissä, mitä seuraa eetterin haihdutus ja pyridiinin tislaus. Suositeltu menetelmä [Lindauer Mukherjee Pure Appl Chem 27 267 1971] kuivaa pyridiinin kiinteällä KOH:lla (20 g/kg) 2 viikon ajan ja tislaa supernatantin jakotislaamalla Linden tyypin 5A molekyyliseulojen ja kiinteän KOH:n yli. Tuotetta säilytetään CO{10}}vapaassa typessä. Pyridiiniä voidaan säilyttää kosketuksessa BaO:n, CaH2:n tai molekyyliseulojen kanssa. Ei-emäksiset materiaalit voidaan poistaa höyrytislaamalla liuosta, joka sisältää 1,2 ekvivalenttia 20 % H2SO4:a tai 17 % HCl:a, kunnes noin 10 % emäksestä on kulkeutunut ei-emäksisten epäpuhtauksien mukana. Sitten jäännös tehdään emäksiseksi ja emäs erotetaan, kuivataan NaOH:lla ja fraktiotislataan. Vaihtoehtoisesti pyridiiniä voidaan käsitellä hapettimilla. Siten pyridiiniä (800 ml) on sekoitettu 24 tunnin ajan seeriinisulfaatin (20 g) ja vedettömän K2C03:n (15 g) seoksen kanssa, sitten suodatettu ja fraktiotislattu. Hurd ja Simon [J Am Chem Soc 84 4519 1962] sekoittivat pyridiiniä (135 ml), vettä (2,5 l) ja KMnO4:a (90 g) 2 tuntia 100 asteessa, sitten seisoivat 15 tuntia ennen kuin saostuneet mangaanioksidit suodattivat pois. Kiinteän KOH:n (noin 500 g) lisääminen sai pyridiinin erottumaan. Se dekantoitiin, palautusjäähdytettiin CaO:n kanssa 3 tuntia ja tislattiin. Pyridiinin erottaminen joistakin sen homologeista voidaan saavuttaa kiteyttämällä oksalaatteja. Pyridiini saostetaan oksalaattina lisäämällä se sekoitettuun oksaalihapon asetoniliuokseen. Sakka suodatetaan, pestään kylmällä asetonilla ja pyridiini regeneroidaan ja eristetään. Muut menetelmät perustuvat kompleksin muodostukseen ZnCl2:n tai HgCl2:n kanssa. |
| Yhteensopimattomuudet | Voimakas reaktio vahvojen hapettimien kanssa; vahvat hapot; kloorisulfonihappo; maleiinihappoanhydridi; oleum jodi. |
| Jätehuolto | Hallittu poltto, jossa typen oksidit poistetaan poistokaasusta pesuri-, katalyytti- tai lämpölaitteilla. |
| Pyridiinivalmisteet ja raaka-aineet |
| Raakamateriaalit | Sulfuric acid-->Ammonia-->Benzene-->COAL TAR-->3-Picoline-->COKEOVENGAS-->1,5-DIAMINOPENTAANIDIHYDROKLORIDI |
| Valmistustuotteet | Methyl 2-Fluoroisonicotinate-->2-ACETYL-5-CYANOTHIOPHENE-->5-BROMO-2-FLUOROCINNAMIC ACID-->4-NITROISOPHTHALIC ACID-->3,5-DIMETHOXYCINNAMIC ACID-->2-(2-Butoxyethoxy)ethyl acetate-->2,4-MESITYLENEDISULFONYL DICHLORIDE-->(4-FLUORO-BENZYL)-METHYL-AMINE-->1-Phenacylpyridinium bromide-->3-(TRIFLUOROMETHOXY)CINNAMIC ACID-->trans-Ferulic acid-->3-(Trifluoromethyl)pyrazole-->4-Fluorocinnamic acid-->Indigosol Green Blue IBC-->2-Amino-4-methyl-5-acetylthiazole-->Benzyl 2-chloroacetate-->5-ACETAMIDONICOTINIC ACID-->7-ACETOXYCOUMARIN-->2-AMINO-4-METHYL-QUINOLINE-3-CARBONITRILE-->N-PHENYLISONICOTINAMIDE-->Allyl methyl carbonate-->Pyridine-3-sulfonyl chloride hydrochloride-->Syringaldehyde-->2,4,5,6-TETRAMETHYLBENZENEDISULFONYL DICHLORIDE-->3-(3-METHYL-2-THIENYL)ACRYLIC ACID-->Vat Grey M-->17beta-Hydroxy-17-methylandrosta-4,9(11)-dien-3-one-->butyl N-phenylcarbamate-->3-Methoxycinnamic acid-->1-CHLORO-2-METHYLPROPYL CHLOROFORMATE-->Pyrazinecarbonitrile-->2-AMINO-6-CHLORO-3,5-DICYANOPYRIDINE-->4-BROMO-TETRAHYDROPYRAN-->Phenylcarbamic acid propyl ester-->Hydrocortisone acetate-->5-METHYLPICOLINIC ACID-->4-Acetamido-2-chloropyridine-->Pyridinium p-Toluenesulfonate-->1,2,4-Triazolo[4,3-a]pyridin-3(2H)-one-->Paraquat dikloridi |
Suositut Tagit: pyridine, Kiina pyridiinin valmistajat, toimittajat, tehdas
Saatat myös pitää
-

Tehdasmyynti CAS 100-06-1 4-metoksiasetofenoni
-

CAS 1335-66-6 Kiinan tehtaalta Isocyclocitralin
-

Elintarvikelaatuiset elintarvikelisäaineet CAS 93-92-5 Styralyyliasetaatti
-

Tehdashinta Paras hinta CAS 577-16-2 2-Metyyliasetofenoni
-

Kilpailukykyinen hinta CAS 624-89-5 Metyylietyylisulfidi
-

2-Etoksikanaftaleeni
Lähetä kysely

